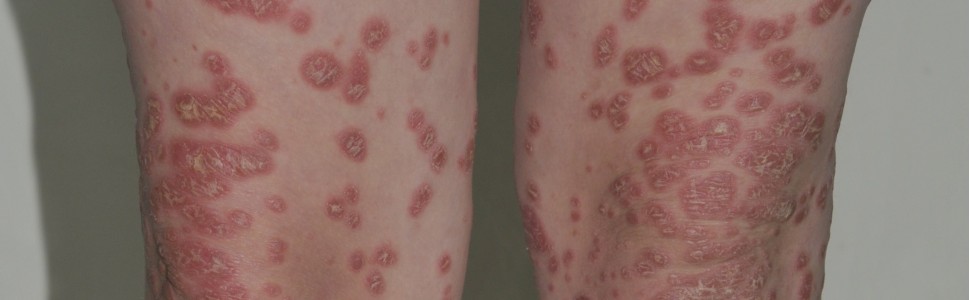
Łuszczyca u dzieci występuje nieco rzadziej niż u dorosłych (najczęściej początek zachorowania obserwuje się u młodych osób dorosłych), zdarzają się jednak przypadki o ciężkim przebiegu, które do osiągnięcia kontroli zmian skórnych wymagają stosowania terapii ogólnych. Wpływ choroby na rozwój emocjonalny, a także w dalszej perspektywie na poczucie własnej wartości i rozwój społeczny dziecka jest ogromny, dlatego należy dążyć do jak najlepszych efektów terapeutycznych.
Na szczęście w ostatnich latach miały były przeprowadzone liczne badania kliniczne, które weryfikują toksyczność systemowych terapii przeciwłuszczycowych, takich jak metotreksat, cyklosporyna A i retinoidy, co zmniejszyło obawy przed ich stosowaniem u dzieci. Ponadto coraz więcej najnowocześniejszych preparatów biologicznych okazuje się być bezpiecznymi i bardzo skutecznymi u dzieci. Do chwili obecnej u dzieci zarejestrowano dwa leki o aktywności anty-TNF-α: etanercept (w 2009 r.) i adalimumab (w 2015 r.).
Na łamach Journal of the American Academy of Dermatology ukazały się właśnie wyniki badania klinicznego III fazy, w którym oceniano bezpieczeństwo i skuteczność ustekinumabu wśród młodzieży w wieku 12-17 lat z umiarkowaną i ciężką łuszczycą pospolitą. Lek ten wykazuje aktywność anty-IL-12/23.
110 pacjentów objętych badaniem randomizowano do 3 grup: otrzymujących standardowe dawkowanie leku, otrzymujących połowę dawki standardowej w schemacie 0,4 tydzień i następnie co 12 tygodni oraz otrzymujących placebo przez pierwszych 12 tygodni badania. Oceniano stan kliniczny w oparciu o skalę Physician Global Assessment (PGA) i skalę PASI.
W 12 tygodniu badania PGA0/1 i PASI75 osiągnięto u odpowiednio: 67,6% i 78,4% chorych otrzymujących połowę dawki standardowej, 69,4% i 80,6% chorych otrzymujących pełną dawkę oraz u 5,4% i 10,8% otrzymujących placebo. Działania niepożądane w pierwszych 12 tygodniach zgłosiło 56,8% pacjentów przyjmujących placebo, 51,4% otrzymujących połowę dawki i 44,4% leczonych pełną dawką leku.
Autorzy wnioskują, że skuteczność leku w badanej populacji jest porównywalna ze skutecznością u dorosłych. W ciągu 1 roku trwania badania nie obserwowano nieoczekiwanych działań ubocznych.
Źródło: http://www.jaad.org/
Lek. Michał Adamczyk
Klinika Dermatologii, Wenerologii i Dermatologii Dziecięcej Uniwersytetu Medycznego w Lublinie